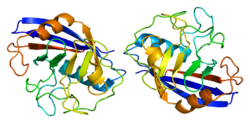| NKTR |
|---|
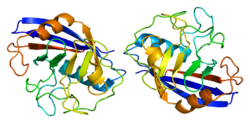 |
| Наявні структури |
|---|
| PDB | Пошук ортологів: PDBe RCSB |
|---|
| |
| Ідентифікатори |
|---|
| Символи | NKTR, p104, natural killer cell triggering receptor |
|---|
| Зовнішні ІД | OMIM: 161565 MGI: 97346 HomoloGene: 122148 GeneCards: NKTR |
|---|
| Онтологія гена |
|---|
| Молекулярна функція | • isomerase activity
• peptidyl-prolyl cis-trans isomerase activity
• cyclosporin A binding
• unfolded protein binding
|
|---|
| Клітинна компонента | • мембрана
• нуклеоплазма
• мітохондрія
• гіалоплазма
• клітинна мембрана
• клітинне ядро
|
|---|
| Біологічний процес | • згортання білків
• protein peptidyl-prolyl isomerization
• protein refolding
|
|---|
| Джерела:Amigo / QuickGO | |
| Шаблон експресії |
|---|
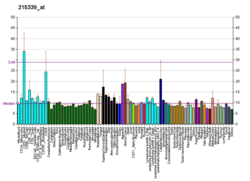 |
| Більше даних |
| Ортологи |
|---|
| Види | Людина | Миша |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (мРНК) | | NM_001012651
NM_005385
NM_001349124
NM_001349125
NM_001349126 |
| |
|---|
| RefSeq (білок) | | NP_005376
NP_001336053
NP_001336054
NP_001336055 |
| |
|---|
| Локус (UCSC) | Хр. 3: 42.6 – 42.65 Mb | Хр. 9: 121.72 – 121.76 Mb |
|---|
| PubMed search | [1] | [2] |
|---|
| Вікідані |
| Див./Ред. для людей | Див./Ред. для мишей |
|
NKTR (англ. Natural killer cell triggering receptor) – білок, який кодується однойменним геном, розташованим у людей на короткому плечі 3-ї хромосоми. [3] Довжина поліпептидного ланцюга білка становить 1 462 амінокислот, а молекулярна маса — 165 677[4].
Послідовність амінокислот
| 10 | | 20 | | 30 | | 40 | | 50 |
|---|
| MGAQDRPQCH | | FDIEINREPV | | GRIMFQLFSD | | ICPKTCKNFL | | CLCSGEKGLG |
| KTTGKKLCYK | | GSTFHRVVKN | | FMIQGGDFSE | | GNGKGGESIY | | GGYFKDENFI |
| LKHDRAFLLS | | MANRGKHTNG | | SQFFITTKPA | | PHLDGVHVVF | | GLVISGFEVI |
| EQIENLKTDA | | ASRPYADVRV | | IDCGVLATKS | | IKDVFEKKRK | | KPTHSEGSDS |
| SSNSSSSSES | | SSESELEHER | | SRRRKHKRRP | | KVKRSKKRRK | | EASSSEEPRN |
| KHAMNPKGHS | | ERSDTNEKRS | | VDSSAKREKP | | VVRPEEIPPV | | PENRFLLRRD |
| MPVVTAEPEP | | KIPDVAPIVS | | DQKPSVSKSG | | RKIKGRGTIR | | YHTPPRSRSC |
| SESDDDDSSE | | TPPHWKEEMQ | | RLRAYRPPSG | | EKWSKGDKLS | | DPCSSRWDER |
| SLSQRSRSWS | | YNGYYSDLST | | ARHSGHHKKR | | RKEKKVKHKK | | KGKKQKHCRR |
| HKQTKKRRIL | | IPSDIESSKS | | STRRMKSSCD | | RERSSRSSSL | | SSHHSSKRDW |
| SKSDKDVQSS | | LTHSSRDSYR | | SKSHSQSYSR | | GSSRSRTASK | | SSSHSRSRSK |
| SRSSSKSGHR | | KRASKSPRKT | | ASQLSENKPV | | KTEPLRATMA | | QNENVVVQPV |
| VAENIPVIPL | | SDSPPPSRWK | | PGQKPWKPSY | | ERIQEMKAKT | | THLLPIQSTY |
| SLANIKETGS | | SSSYHKREKN | | SESDQSTYSK | | YSDRSSESSP | | RSRSRSSRSR |
| SYSRSYTRSR | | SLASSHSRSR | | SPSSRSHSRN | | KYSDHSQCSR | | SSSYTSISSD |
| DGRRAKRRLR | | SSGKKNSVSH | | KKHSSSSEKT | | LHSKYVKGRD | | RSSCVRKYSE |
| SRSSLDYSSD | | SEQSSVQATQ | | SAQEKEKQGQ | | MERTHNKQEK | | NRGEEKSKSE |
| RECPHSKKRT | | LKENLSDHLR | | NGSKPKRKNY | | AGSKWDSESN | | SERDVTKNSK |
| NDSHPSSDKE | | EGEATSDSES | | EVSEIHIKVK | | PTTKSSTNTS | | LPDDNGAWKS |
| SKQRTSTSDS | | EGSCSNSENN | | RGKPQKHKHG | | SKENLKREHT | | KKVKEKLKGK |
| KDKKHKAPKR | | KQAFHWQPPL | | EFGEEEEEEI | | DDKQVTQESK | | EKKVSENNET |
| IKDNILKTEK | | SSEEDLSGKH | | DTVTVSSDLD | | QFTKDDSKLS | | ISPTALNTEE |
| NVACLQNIQH | | VEESVPNGVE | | DVLQTDDNME | | ICTPDRSSPA | | KVEETSPLGN |
| ARLDTPDINI | | VLKQDMATEH | | PQAEVVKQES | | SMSESKVLGE | | VGKQDSSSAS |
| LASAGESTGK | | KEVAEKSQIN | | LIDKKWKPLQ | | GVGNLAAPNA | | ATSSAVEVKV |
| LTTVPEMKPQ | | GLRIEIKSKN | | KVRPGSLFDE | | VRKTARLNRR | | PRNQESSSDE |
| QTPSRDDDSQ | | SRSPSRSRSK | | SETKSRHRTR | | SVSYSHSRSR | | SRSSTSSYRS |
| RSYSRSRSRG | | WYSRGRTRSR | | SSSYRSYKSH | | RTSSRSRSRS | | SSYDPHSRSR |
| SYTYDSYYSR | | SRSRSRSQRS | | DSYHRGRSYN | | RRSRSCRSYG | | SDSESDRSYS |
| HHRSPSESSR | | YS |
Кодований геном білок за функціями належить до ізомераз, ротамаз, фосфопротеїнів. Задіяний у такому біологічному процесі як поліморфізм. Локалізований у мембрані.
Література
- Impens F., Radoshevich L., Cossart P., Ribet D. (2014). Mapping of SUMO sites and analysis of SUMOylation changes induced by external stimuli. Proc. Natl. Acad. Sci. U.S.A. 111: 12432—12437. PMID 25114211 DOI:10.1073/pnas.1413825111
- Hendriks I.A., Treffers L.W., Verlaan-de Vries M., Olsen J.V., Vertegaal A.C. (2015). SUMO-2 orchestrates chromatin modifiers in response to DNA damage. Cell Rep. 10: 1778—1791. PMID 25772364 DOI:10.1016/j.celrep.2015.02.033
Примітки
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:7833 (англ.) . Процитовано 30 серпня 2017.
- ↑ UniProt, P30414 (англ.) . Архів оригіналу за 15 вересня 2016. Процитовано 30 серпня 2017.
Див. також
 | Це незавершена стаття про білки.
Ви можете допомогти проєкту, виправивши або дописавши її. |
 Портал «Біологія» Портал «Біологія»  Портал «Хімія» Портал «Хімія»
|
| На цю статтю не посилаються інші статті Вікіпедії. Будь ласка розставте посилання відповідно до прийнятих рекомендацій. |