| FLII |
|---|
|
| Ідентифікатори |
|---|
| Символи | FLII, FLI, FLIL, Fli1, actin remodeling protein, FLII actin remodeling protein |
|---|
| Зовнішні ІД | OMIM: 600362 MGI: 1342286 HomoloGene: 11092 GeneCards: FLII |
|---|
| Онтологія гена |
|---|
| Молекулярна функція | • actin binding
• GO:0001948, GO:0016582 protein binding
• actin filament binding
|
|---|
| Клітинна компонента | • міжклітинні контакти
• цитоскелет
• brush border
• клітинне ядро
• focal adhesion
• нуклеоплазма
• центр організації мікротрубочок
• цитоплазма
• гіалоплазма
|
|---|
| Біологічний процес | • multicellular organism development
• actin filament severing
• GO:0009373 regulation of transcription, DNA-templated
• actin cytoskeleton organization
• transcription, DNA-templated
|
|---|
| Джерела:Amigo / QuickGO | |
| Шаблон експресії |
|---|
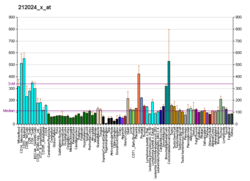

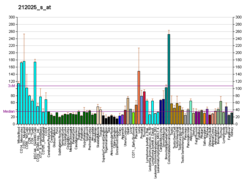 |
| Більше даних |
| Ортологи |
|---|
| Види | Людина | Миша |
|---|
| Entrez | | |
|---|
| Ensembl | | ENSG00000177731
ENSG00000284571 |
| |
|---|
| UniProt | | |
|---|
| RefSeq (мРНК) | | NM_001256264
NM_001256265
NM_002018 |
| |
|---|
| RefSeq (білок) | | NP_001243193
NP_001243194
NP_002009 |
| |
|---|
| Локус (UCSC) | Хр. 17: 18.24 – 18.26 Mb | Хр. 11: 60.6 – 60.62 Mb |
|---|
| PubMed search | [1] | [2] |
|---|
| Вікідані |
| Див./Ред. для людей | Див./Ред. для мишей |
|
FLII (англ. FLII, actin remodeling protein) – білок, який кодується однойменним геном, розташованим у людей на короткому плечі 17-ї хромосоми.[3] Довжина поліпептидного ланцюга білка становить 1 269 амінокислот, а молекулярна маса — 144 751[4].
Послідовність амінокислот
| 10 | | 20 | | 30 | | 40 | | 50 |
|---|
| MEATGVLPFV | | RGVDLSGNDF | | KGGYFPENVK | | AMTSLRWLKL | | NRTGLCYLPE |
| ELAALQKLEH | | LSVSHNNLTT | | LHGELSSLPS | | LRAIVARANS | | LKNSGVPDDI |
| FKLDDLSVLD | | LSHNQLTECP | | RELENAKNML | | VLNLSHNSID | | TIPNQLFINL |
| TDLLYLDLSE | | NRLESLPPQM | | RRLVHLQTLV | | LNGNPLLHAQ | | LRQLPAMTAL |
| QTLHLRSTQR | | TQSNLPTSLE | | GLSNLADVDL | | SCNDLTRVPE | | CLYTLPSLRR |
| LNLSSNQITE | | LSLCIDQWVH | | VETLNLSRNQ | | LTSLPSAICK | | LSKLKKLYLN |
| SNKLDFDGLP | | SGIGKLTNLE | | EFMAANNNLE | | LVPESLCRCP | | KLRKLVLNKN |
| HLVTLPEAIH | | FLTEIEVLDV | | RENPNLVMPP | | KPADRAAEWY | | NIDFSLQNQL |
| RLAGASPATV | | AAAAAAGSGP | | KDPMARKMRL | | RRRKDSAQDD | | QAKQVLKGMS |
| DVAQEKNKKQ | | EESADARAPS | | GKVRRWDQGL | | EKPRLDYSEF | | FTEDVGQLPG |
| LTIWQIENFV | | PVLVEEAFHG | | KFYEADCYIV | | LKTFLDDSGS | | LNWEIYYWIG |
| GEATLDKKAC | | SAIHAVNLRN | | YLGAECRTVR | | EEMGDESEEF | | LQVFDNDISY |
| IEGGTASGFY | | TVEDTHYVTR | | MYRVYGKKNI | | KLEPVPLKGT | | SLDPRFVFLL |
| DRGLDIYVWR | | GAQATLSSTT | | KARLFAEKIN | | KNERKGKAEI | | TLLVQGQELP |
| EFWEALGGEP | | SEIKKHVPED | | FWPPQPKLYK | | VGLGLGYLEL | | PQINYKLSVE |
| HKQRPKVELM | | PRMRLLQSLL | | DTRCVYILDC | | WSDVFIWLGR | | KSPRLVRAAA |
| LKLGQELCGM | | LHRPRHATVS | | RSLEGTEAQV | | FKAKFKNWDD | | VLTVDYTRNA |
| EAVLQSPGLS | | GKVKRDAEKK | | DQMKADLTAL | | FLPRQPPMSL | | AEAEQLMEEW |
| NEDLDGMEGF | | VLEGKKFARL | | PEEEFGHFYT | | QDCYVFLCRY | | WVPVEYEEEE |
| KKEDKEEKAE | | GKEGEEATAE | | AEEKQPEEDF | | QCIVYFWQGR | | EASNMGWLTF |
| TFSLQKKFES | | LFPGKLEVVR | | MTQQQENPKF | | LSHFKRKFII | | HRGKRKAVQG |
| AQQPSLYQIR | | TNGSALCTRC | | IQINTDSSLL | | NSEFCFILKV | | PFESEDNQGI |
| VYAWVGRASD | | PDEAKLAEDI | | LNTMFDTSYS | | KQVINEGEEP | | ENFFWVGIGA |
| QKPYDDDAEY | | MKHTRLFRCS | | NEKGYFAVTE | | KCSDFCQDDL | | ADDDIMLLDN |
| GQEVYMWVGT | | QTSQVEIKLS | | LKACQVYIQH | | MRSKEHERPR | | RLRLVRKGNE |
| QHAFTRCFHA | | WSAFCKALA |
Кодований геном білок за функціями належить до активаторів, білків розвитку, фосфопротеїнів. Задіяний у таких біологічних процесах, як транскрипція, регуляція транскрипції, ацетилювання, альтернативний сплайсинг. Білок має сайт для зв'язування з молекулою актину. Локалізований у цитоплазмі, цитоскелеті, ядрі, клітинних контактах.
Література
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Liu Y.-T., Yin H.L. (1998). Identification of the binding partners for flightless I, a novel protein bridging the leucine-rich repeat and the gelsolin superfamilies. J. Biol. Chem. 273: 7920—7927. PMID 9525888 DOI:10.1074/jbc.273.14.7920
- Wilson S.A., Brown E.C., Kingsman A.J., Kingsman S.M. (1998). TRIP: a novel double stranded RNA binding protein which interacts with the leucine rich repeat of flightless I. Nucleic Acids Res. 26: 3460—3467. PMID 9671805 DOI:10.1093/nar/26.15.3460
- Fong K.S.K., de Couet H.G. (1999). Novel proteins interacting with the leucine-rich repeat domain of human flightless-I identified by the yeast two-hybrid system. Genomics. 58: 146—157. PMID 10366446 DOI:10.1006/geno.1999.5817
- Lee Y.-H., Campbell H.D., Stallcup M.R. (2004). Developmentally essential protein flightless I is a nuclear receptor coactivator with actin binding activity. Mol. Cell. Biol. 24: 2103—2117. PMID 14966289 DOI:10.1128/MCB.24.5.2103-2117.2004
- Beausoleil S.A., Villen J., Gerber S.A., Rush J., Gygi S.P. (2006). A probability-based approach for high-throughput protein phosphorylation analysis and site localization. Nat. Biotechnol. 24: 1285—1292. PMID 16964243 DOI:10.1038/nbt1240
Примітки
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:3750 (англ.) . Процитовано 12 вересня 2017.
{{cite web}}: Обслуговування CS1: Сторінки з параметром url-status, але без параметра archive-url (посилання) - ↑ UniProt, Q13045 (англ.) . Архів оригіналу за 5 вересня 2017. Процитовано 12 вересня 2017.
Див. також
 | Це незавершена стаття про білки.
Ви можете допомогти проєкту, виправивши або дописавши її. |
 Портал «Біологія» Портал «Біологія»  Портал «Хімія» Портал «Хімія»
|














