Фторид плутония(VI)
| Фторид плутония(VI) | |
|---|---|
 | |
| Общие | |
| Систематическое наименование | Фторид плутония(VI) |
| Традиционные названия | гексафторид плутония |
| Хим. формула | PuF6 |
| Физические свойства | |
| Состояние | красно-коричневые кристаллы |
| Молярная масса | 356,06 (239Pu) г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 52 °C |
| • кипения | 62,3 °C |
| Энтальпия | |
| • образования | -1861 кДж/моль |
| Структура | |
| Кристаллическая структура | Pnma (№ 62) |
| Классификация | |
| Рег. номер CAS | 13693-06-6 |
| PubChem | 51880988 |
| SMILES | F[Pu](F)(F)(F)(F)F |
| InChI | InChI=1S/6FH.Pu/h6*1H;/q;;;;;;+6/p-6 OJSBUHMRXCPOJV-UHFFFAOYSA-H |
| ChemSpider | 452599 и 21259382 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
 Медиафайлы на Викискладе Медиафайлы на Викискладе | |
Фтори́д плуто́ния(VI) — неорганическое соединение, соль металла плутония и плавиковой кислоты с формулой PuF6, легкоплавкие красно-коричневые кристаллы, реагирует с водой. Очень сильный окислитель.
Применяется в ядерной промышленности.
Получение
Обычный способ получения гексафторида плутония — эндотермическая реакция окисления тетрафторида плутония () элементарным фтором[1] [2]:
Реакция происходит достаточно быстро при температуре 750 °C, для достижения высокого выхода продукта необходимо быстро сконденсировать гексафторид плутония для снижения скорости обратной реакции распада на реагенты[5].
Физические свойства
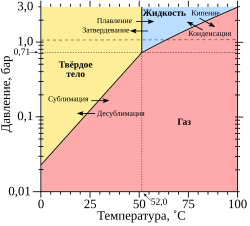
При температуре −180 °C в вакууме, гексафторид плутония — бесцветное кристаллическое вещество, похожее на гексафторид урана, при комнатной температуре вещество представляет собой легкоплавкие красно-коричневые кристаллы, цветом напоминающие по цвету диоксид азота. В жидком виде — прозрачная тёмно-коричневая жидкость[1]. Как и гексафторид урана, гексафторид плутония весьма летуч.
При нормальном давлении (101,325 кПа) плавится при 52 °C и кипит при 62 °C. Тройная точка, при которой три фазы твердой, жидкая и газообразная находятся в равновесии 51,58 °C (324,74 К) при давлении 71 кПа (533 мм рт.ст.), ниже этого давления испаряется не переходя в жидкое состояние (сублимация)[2].
Гексафторид плутония является ковалентным соединением, а не солью с ионными связями в молекуле. Кристаллизуется в орторомбической кристаллической сингонии в пространственной группе Pnma (№ 62) с параметрами решетки a = 995 пм, b = 902 пм и c = 526 пм[1].
В газообразном состоянии состоит из правильных октаэдрических молекул с равными длинами связей Pu-F 197,1 пм[6].
Химические свойства
Реагирует с водой с образованием фторида плутонила и фтороводорода[2][7]:
- .
Эта реакция медленно протекает при нахождении гексафторида плутония во влажном воздухе, поэтому его хранят в запаянных кварцевых ампулах.
Растворим в серной кислоте.
Вследствие радиоактивности и α-излучения плутония его гексафторид постоянно подвергается радиолизу с образованием нелетучих фторидов плутония в низких степенях окисления и выделением элементного фтора, благодаря чему используется для фторирования различных веществ:
- .
Применение
В ядерной промышленности, для разделения изотопов плутония на газовых центрифугах.
Примечания
- ↑ 1 2 3 C. J. Mandleberg, H. K. Rae, R. Hurst, G. Long, D. Davies, K. E. Francis: Plutonium Hexafluoride, in: Journal of Inorganic and Nuclear Chemistry, 1956, 2 (5-6), S. 358—367 (doi:10.1016/0022-1902(56)80090-0).
- ↑ 1 2 3 Alan E. Florin, Irving R. Tannenbaum, Joe F. Lemons: Preparation and Properties of Plutonium Hexafluoride and Identification of Plutonium(VI) Oxyfluoride, in: Journal of Inorganic and Nuclear Chemistry, 1956, 2 (5-6), S. 368—379 (doi:10.1016/0022-1902(56)80091-2).
- ↑ M. J. Steindler, D. V. Steidl, R. K. Steunenberg: The Fluorination of Plutonium Tetrafluoride (Argonne National Laboratory Report ANL-5875); 1. Juni 1958 (Abstract Архивная копия от 5 марта 2016 на Wayback Machine).
- ↑ M. J. Steindler, D. V. Steidl, R. K. Steunenberg: The Fluorination of Plutonium Tetrafluoride and Plutonium Dioxide by Fluorine, in: Nucl. Sci. and Eng., 1959, 6 (4), S. 333—340 (Abstract Архивная копия от 5 марта 2016 на Wayback Machine).
- ↑ Bernard Weinstock, John G. Malm: The Properties of Plutonium Hexafluoride, in: Journal of Inorganic and Nuclear Chemistry, 1956, 2 (5-6), S. 380—394 (doi:10.1016/0022-1902(56)80092-4).
- ↑ Masao Kimura, Werner Schomaker, Darwin W. Smith, Bernard Weinstock: Electron-Diffraction Investigation of the Hexafluorides of Tungsten, Osmium, Iridium, Uranium, Neptunium, and Plutonium, in: J. Chem. Phys., 1968, 48 (8), S. 4001–4012 (doi:10.1063/1.1669727).
- ↑ R. W. Kessie: Plutonium and Uranium Hexafluoride Hydrolysis Kinetics, in: Ind. Eng. Chem. Proc. Des. Dev., 1967, 6 (1), S. 105–111 (doi:10.1021/i260021a018).
Литература
- Некрасов Б. В. Основы общей химии — Т. 2. — М.: Химия, 1973
- Успехи химии. — 1966. — Т. 35, № 12.
- Успехи химии. — 1971. — Т. 40, № 2.
| HF DF | He | ||||||||||||||||
| LiF | BeF2 | BF3 | CF4 | N2F2 N2F4 NF3 NH4F | O4F2 O2F2 OF2 | F | Ne | ||||||||||
| NaF | MgF2 | AlF3 | SiF2 Si3F8 Si4F10 SiF4 | PF3 PF5 | S2F2 SF4 S2F10 SF6 | ClF ClF3 ClF5 | Ar | ||||||||||
| KF | CaF2 | ScF3 | TiF2 TiF3 TiF4 | VF2 VF3 VF4 VF5 | CrF2 СrF3 СrF4 СrF5 | MnF2 MnF3 MnF4 | FeF2 FeF3 | CoF2 CoF3 | NiF2 NiF4 | CuF CuF2 | ZnF2 | GaF3 | GeF2 GeF4 | AsF3 AsF5 | SeF4 SeF6 | BrF BrF3 BrF5 | KrF2 KrF4 |
| RbF | SrF2 | YF3 | ZrF2 ZrF3 ZrF4 | NbF3 NbF4 NbF5 | MoF3 MoF5 MoF6 | TcF5 TcF6 | RuF3 RuF5 RuF6 | RhF3 RhF4 RhF5 RhF6 | PdF2 PdF3 PdF4 | AgF AgF2 | CdF2 | InF3 | SnF2 SnF4 | SbF3 SbF5 | TeF4 TeF6 | IF IF3 IF5 IF7 | XeF2 XeF4 |
| CsF | BaF2 | HfF4 | TaF5 | WF4 WF5 WF6 | ReF4 ReF5 ReF6 ReF7 | OsF4 OsF5 OsF6 OsF7 OsF8 | IrF3 IrF4 IrF5 IrF6 | PtF2 PtF4 PtF5 PtF6 | Au4F8 AuF3 AuF5 AuF5·F2 | Hg2F2 HgF2 | TlF TlF3 | PbF2 PbF4 | BiF3 BiF5 | Po | At | Rn | |
| Fr | RaF2 | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| ↓ | |||||||||||||||||
| LaF3 | CeF3 CeF4 | PrF3 PrF4 | NdF3 | Pm | SmF2 SmF3 | EuF2 EuF3 | GdF3 | Tb | DyF3 | HoF3 | Er | Tm | YbF2 YbF3 | LuF3 | |||
| AcF3 | ThF4 | PaF4 PaF5 | UF3 UF4 UF5 UF6 | NpF3 NpF4 NpF5 NpF6 | PuF3 PuF4 PuF6 | Am | CmF3 | BkF4 | Cf | Es | Fm | Md | No | Lr | |||














