Claudina

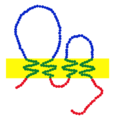
Claudinas são uma família de proteínas que são os componentes mais importantes das junções oclusivas (impermeabilizantes), onde estabelecem a barreira paracelular que controla o fluxo de moléculas no espaço intercelular entre as células de um epitélio. Possuem quatro domínios transmembranares, com os terminais amina e carboxilo no citoplasma.
Estrutura
As claudinas são proteínas transmembranares pequenas (20–27 kilodalton (kDa)) que se encontram em muitos organismos, desde nematóides a seres humanos, e são muito semelhantes em termos de estrutura, apesar desta conservação não se observar a nível genético. As claudinas atravessam a membrana citoplasmática 4 vezes, com ambos os terminais, amina e carboxilo, localizados no citoplasma e dois loops extracelulares. O primeiro loop extracelular tem, em média, 53 aminoácidos e o segundo, ligeiramente mais pequeno, 24 aminoácidos. O terminal amina é habitualmente muito curto (4-10 aminoácidos). O terminal carboxilo varia entre 21 e 63 aminoácidos e é necessário para a localização destas proteínas nas junções oclusivas.[1] Suspeita-se que as cisteínas de claudinas individuais ou separadas formam ligações dissulfureto. Todas as claudinas humanas (exceto a claudina 12) possuem domínios que as permitem ligar-se a domínios PDZ.
Genes
Em humanos, foram descritos 24 membros da família.
- CLDN1, CLDN2, CLDN3, CLDN4, CLDN5, CLDN6, CLDN7, CLDN8, CLDN9, CLDN10, CLDN11, CLDN12, CLDN13, CLDN14, CLDN15, CLDN16, CLDN17, CLDN18, CLDN19, CLDN20, CLDN21, CLDN22, CLDN23
Ver também
- Ocludina