염화 니켈(II)
 | |
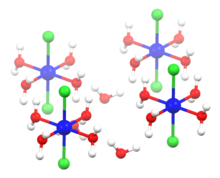 structure of hexahydrate | |
 Anhydrous | |
| 이름 | |
|---|---|
| IUPAC 이름 Nickel(II) chloride | |
| 별칭 Nickelous chloride, nickel(II) salt of hydrochloric acid | |
| 식별자 | |
| |
3D 모델 (JSmol) |
|
| ChEBI |
|
| ChemSpider |
|
| ECHA InfoCard | 100.028.858 |
| EC 번호 |
|
| KEGG |
|
PubChem CID |
|
| RTECS 번호 |
|
| UNII |
|
| UN 번호 | 3288 3077 |
CompTox Dashboard (EPA) |
|
| |
SMILES
| |
| 성질 | |
| NiCl2 | |
| 몰 질량 | 129.5994 g/mol (anhydrous) 237.69 g/mol (hexahydrate) |
| 겉보기 | yellow-brown crystals deliquescent (anhydrous) green crystals (hexahydrate) |
| 냄새 | odorless |
| 밀도 | 3.55 g/cm3 (anhydrous) 1.92 g/cm3 (hexahydrate) |
| 녹는점 | 1,001 °C (1,834 °F; 1,274 K) (anhydrous) 140 °C (hexahydrate) |
| anhydrous 67.5 g/100 mL (25 °C)[1] 87.6 g/100 mL (100 °C) hexahydrate 282.5 g/100 mL (25 °C)[1] 578.5 g/100 mL (100 °C) | |
| 용해도 | 0.8 g/100 mL (hydrazine) soluble in ethylene glycol, ethanol, ammonium hydroxide insoluble in ammonia, nitric acid |
| 산성도 (pKa) | 4 (hexahydrate) |
자화율 (χ) | +6145.0·10−6 cm3/mol |
| 구조 | |
| Monoclinic | |
배위 기하 구조 | octahedral at Ni |
| 열화학 | |
표준 몰 엔트로피 (S | 107 J·mol−1·K−1[2] |
표준 생성 엔탈피 (ΔfH⦵298) | −316 kJ·mol−1[2] |
| 위험 | |
| 주요 위험 | Very toxic (T+) Irritant (Xi) Dangerous for the environment (N) Carcinogen |
| 물질 안전 보건 자료 | Fischer Scientific |
| GHS 그림문자 |    |
| 신호어 | 위험 |
GHS 유해위험문구 | H301, H315, H317, H331, H334, H341, H350i, H360D, H372, H410 |
GHS 예방조치문구 | P201, P202, P260, P261, P264, P270, P271, P272, P273, P280, P281, P285, P301+310, P302+352, P304+340, P304+341, P308+313, P311, P314, P321, P330, P332+313, P333+313, P342+311, P362 |
| NFPA 704 (파이어 다이아몬드) |  0 3 0 |
| 인화점 | Non-flammable |
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |
LD50 (median dose) | 105 mg/kg (rat, oral)[3] |
| 관련 화합물 | |
다른 음이온 | Nickel(II) fluoride Nickel(II) bromide Nickel(II) iodide |
다른 양이온 | Palladium(II) chloride Platinum(II) chloride Platinum(II,IV) chloride Platinum(IV) chloride |
관련 화합물 | Cobalt(II) chloride Copper(II) chloride |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.  아니오 확인 (관련 정보 아니오 확인 (관련 정보  예 예 아니오 ?) 아니오 ?) 정보상자 각주 | |
염화 니켈(II)(Nickel(II) chloride) 또는 염화 니켈은 화합물 NiCl2이다. 무수염은 노란색이지만 더 친숙한 수화물 NiCl2·6H2O는 녹색이다. 다양한 형태의 염화 니켈(II)는 화학적 합성을 위한 니켈의 가장 중요한 공급원이다. 염화니켈은 조해성이며 공기로부터 수분을 흡수하여 용액을 형성한다. 니켈염은 장기간 흡입 노출의 경우 폐와 비강에 발암성이 있는 것으로 나타났다.
안전
염화 니켈(II)은 섭취, 흡입, 피부 접촉 및 눈 접촉 시 자극적이다. 니켈과 그 화합물에 대한 장기간 흡입 노출은 폐와 비강의 암 위험 증가와 관련이 있다.
각주
- ↑ 가 나 Lide, David S. (2003). 《CRC Handbook of Chemistry and Physics, 84th Edition》. CRC Press. 4–71쪽. ISBN 9780849304842.
- ↑ 가 나 Zumdahl, Steven S. (2009). 《Chemical Principles 6th Ed.》. Houghton Mifflin Company. A22쪽. ISBN 978-0-618-94690-7.
- ↑ “Nickel metal and other compounds (as Ni)”. 《Immediately Dangerous to Life and Health Concentrations (IDLH)》. National Institute for Occupational Safety and Health (NIOSH).
외부 링크
- NIOSH Pocket Guide to Chemical Hazards
- Linstrom, Peter J.; Mallard, William G. (eds.); NIST Chemistry WebBook, NIST Standard Reference Database Number 69, National Institute of Standards and Technology, Gaithersburg (MD), http://webbook.nist.gov
- v
- t
- e
염화물(Cl-)
| HCl(aq) | He | ||||||||||||||||||||
| LiCl | BeCl2 | BCl3 B2Cl4 +BO3 | C2Cl2 C2Cl4 C2Cl6 CCl4 | NCl3 ClN3 | ClxOy Cl2O Cl2O2 ClO ClO2 Cl2O4 Cl2O6 Cl2O7 ClO4 | ClF ClF3 ClF5 | Ne | ||||||||||||||
| NaCl | MgCl2 | AlCl AlCl3 | Si2Cl6 SiCl4 | P2Cl4 PCl3 PCl5 | S2Cl2 SCl2 SCl4 | Cl2 | Ar | ||||||||||||||
| KCl | CaCl CaCl2 | ScCl3 | TiCl2 TiCl3 TiCl4 | VCl2 VCl3 VCl4 VCl5 | CrCl2 CrCl3 CrCl4 | MnCl2 MnCl3 | FeCl2 FeCl3 | CoCl2 CoCl3 | NiCl2 | CuCl CuCl2 | ZnCl2 | GaCl GaCl3 | GeCl2 GeCl4 | AsCl3 AsCl5 | Se2Cl2 SeCl2 SeCl4 | BrCl | Kr | ||||
| RbCl | SrCl2 | YCl3 | ZrCl3 ZrCl4 | NbCl3 NbCl4 NbCl5 | MoCl2 MoCl3 MoCl4 MoCl5 MoCl6 | TcCl3 TcCl4 | RuCl2 RuCl3 RuCl4 | RhCl3 | PdCl2 | AgCl | CdCl2 | InCl InCl2 InCl3 | SnCl2 SnCl4 | SbCl3 SbCl5 | Te3Cl2 TeCl2 TeCl4 | ICl ICl3 | XeCl XeCl2 XeCl4 | ||||
| CsCl | BaCl2 | * | LuCl3 | HfCl4 | TaCl5 | WCl2 WCl3 WCl4 WCl5 WCl6 | ReCl3 ReCl4 ReCl5 ReCl6 | OsCl2 OsCl3 OsCl4 OsCl5 | IrCl2 IrCl3 IrCl4 | PtCl2 PtCl4 | AuCl (Au[AuCl4])2 AuCl3 | Hg2Cl2 HgCl2 | TlCl TlCl3 | PbCl2 PbCl4 | BiCl3 | PoCl2 PoCl4 | AtCl | Rn | |||
| FrCl | RaCl2 | ** | LrCl3 | RfCl4 | DbCl5 | SgO2Cl2 | BhO3Cl | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||
| * | LaCl3 | CeCl3 | PrCl3 | NdCl2 NdCl3 | PmCl3 | SmCl2 SmCl3 | EuCl2 EuCl3 | GdCl3 | TbCl3 | DyCl2 DyCl3 | HoCl3 | ErCl3 | TmCl2 TmCl3 | YbCl2 YbCl3 | |||||||
| ** | AcCl3 | ThCl4 | PaCl4 PaCl5 | UCl3 UCl4 UCl5 UCl6 | NpCl3 | PuCl3 | AmCl2 AmCl3 | CmCl3 | BkCl3 | CfCl3 | EsCl2 EsCl3 | FmCl2 | MdCl2 | NoCl2 | |||||||




