SOX6
| SOX6 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifiants | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Aliases | SOX6, Protéine SOX6 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| IDs externes | OMIM: 607257 MGI: 98368 HomoloGene: 22631 GeneCards: SOX6 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Wikidata | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
La protéine SOX6 fait partie de la famille des protéines SOX, plus précisément du sous-groupe D avec SOX5 et 13. Cette famille de protéines tire son nom de SRY (Sex determining Region on Y-box). Cette famille a été nommée ainsi à cause du domaine HMG (High Mobility Group) qu’elle possède et qui est très semblable à celui de SRY, le gène codant la différenciation des gonades en testicules chez les embryons mâles. Les SOX sont des facteurs de transcription qui jouent un rôle très important dans l’embryogenèse et dans la destinée des cellules non différenciées.
Domaine HMG
Le domaine HMG (High Mobility Group) est présent chez plusieurs familles de facteurs de transcription. Ce domaine, chez les protéines, entre en interaction avec la petite dépression de l’ADN (voir la figure 1) pour former une courbure de 70-85 o qui facilitera par la suite la transcription de l’ADN. La protéine SOX6, pour sa part, reconnaît, grâce à son domaine HMG, le motif 5’-AACAAT-3’ de l’ADN.
Gène codant SOX6
Le gène codant SOX6 a été isolé pour la première fois d’une banque d’ADNc (ADN complémentaire) de testicule de souris adulte. Il se retrouve sur le chromosome 7 murin (partie distale) ou sur le chromosome 11 humain (11p15.2-15.3) (voir la figure 2) (localisation). Le gène humain possède 16 exons qui ne sont pas toujours tous exprimés puisque l’ARNm de SOX6 subit un épissage alternatif conduisant possiblement à trois bouts : le premier, d’environ 3kpb (kilo-bases) est retrouvé dans les testicules uniquement ; le second, d’environ 8 à 9kpb se trouve un peu partout dans l’organisme ; et le dernier est très peu connu à ce jour.
Les gènes des protéines SOX sont très conservés à travers le règne animal et cela à cause de leur rôle important dans la formation embryonnaire. En effet, la truite arc-en-ciel possède, elle aussi pour SOX6, des bouts de 3kpb et 10kpb. Par contre, SOX6 possède une grande homologie avec SOX5 ce qui permet de supposer qu’il proviendrait d’une mauvaise ségrégation de chromosomes lors de la réplication cellulaire et donc, qu’il serait un gène apparu plus récemment dans l’évolution.
L’ADNc de SOX6 de souris possède 94,3 % d’homologie avec celui de l’humain et leurs domaines HMG sont parfaitement identiques. Ainsi, l’étude de SOX6 avec le gène murin permet de croire que des résultats très similaires seraient obtenus si le gène humain était lui-même étudié. D’ailleurs, la souris p100H qui possède une mutation dans son gène SOX6 est un sujet idéal pour l’étude des effets de ce facteur de transcription.
Actions de la protéine SOX6
La protéine SOX6 entre régulièrement en interaction avec des cofacteurs. Ainsi, elle forme des homo/hétérodimères qui ont soit une action activatrice soit une action inhibitrice dépendant du cofacteur lié. Par exemple, la liaison SOX6-SOX5 avec l’action de SOX9 active le gène du collagène de type 2 pour permettre la formation du cartilage dans la chondrogenèse. D’un autre côté, SOX6-CtBp2 (C-terminal binding protein), une fois liée, réprime le gène Fgf-3 (Fibroblast growth factor) un facteur de croissance pouvant conduire à l’hypertrophie cellulaire s’il est mal régulé.
Lieux d’action de la protéine SOX6

Le morceau de 8 à 9kpb de SOX6 est retrouvé à travers tout l’organisme dans des proportions variant selon l’endroit. Le bout de 3kpb, tel que mentionné précédemment, est présent dans les testicules seulement. Ainsi, la protéine provenant de l’ARNm de 8 à 9kpb est impliquée de façon importante dans la chondrogenèse, le développement de la musculature squelettique et cardiaque, dans l’érythropoïèse et dans d’autres phénomènes encore peu étudiés.
La chondrogenèse normale est expliquée grâce à un schéma très général (voir figure 3). Lorsque la protéine SOX6 est inactivée, comme c’est le cas dans la souris p100H, SOX5 peut compenser ce qui donne, à la naissance, une souris possédant des déficiences osseuses mais elle est viable pour quelque temps. Par contre, si SOX6 et SOX5 sont tous deux absents, la souris meure in utero à cause d’une achondrogenèse généralisée. Ainsi, SOX6 est un facteur de transcription important dans la formation du cartilage et par le fait même dans l’ossification de l’embryon en développement.
SOX6 est aussi impliquée dans la formation des muscles cardiaque et squelettiques. En effet, SOX6 liée à Prtb (Proline-rich transcript of brain) régule cette fois-ci la transcription du gène α1c qui code une partie du canal calcique de type L. Ce canal est d’une importance primordiale dans la contraction cardiaque. En l’absence de SOX6, les souris qui naissent démontrent un bloc atrio-ventriculaire partiel, parfois complet, et présentent des battements cardiaques anormalement lents. Une analyse des cellules cardiaque montre aussi une augmentation du nombre de mitochondries dans la cellule, ainsi que de grosses vacuoles et des dépôts lipidiques. Ces signes sont habituellement typiques des myopathies humaines. Pour ce qui est des cellules musculaires squelettiques, elles présentent aussi des dépôts, possèdent des noyaux irréguliers et plissés et les fibres sont très minces et parfois liquéfiées (détruites).
La protéine SOX6 est aussi très importante dans l’érythropoïèse. Ce facteur de transcription permet, grâce à l’activation des bons gènes, d’augmenter le temps de survie de l’érythropoïétine (Epo), il stimule aussi la prolifération cellulaire quantitativement et qualitativement et favorise la maturation finale des globules rouges en permettant une meilleure acquisition de l’hémoglobine et en facilitant l’éjection du noyau. Les fœtus de souris ne possédant pas SOX6 présentent beaucoup d’érythrocytes nucléés dans leur sang, souffrent habituellement d’anémie et ont un taux de survie plutôt bas. Ils ont par ailleurs un faible développement de leurs organes érythroprogéniteurs (foie, rate, moelle osseuse) jusqu’à ce que l’Epo les hypertrophie pour augmenter leur production de globules rouges.
Finalement, SOX6 est aussi retrouvé dans les testicules de souris adultes et dans leur système nerveux central (SNC), mais son rôle exact à ces deux endroits est mal compris. De plus, cette protéine est présente dans les gliomes et des études sont menées pour déterminer si elle pourrait servir au développement et à la mise en marché d’un test de dépistage.
Pistes de recherche
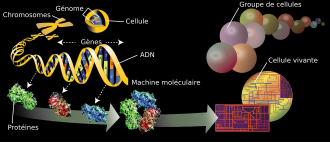
La famille des SOX est un groupe de facteur de transcription en pleine expansion et leur étude est d’un grand intérêt pour comprendre le développement fœtal ainsi que les voies de différenciation des cellules souches. Pour ce qui est de SOX6 en particulier, c’est une protéine qu’il serait très intéressant de connaître davantage puisqu’elle semble être très polyvalente et de tous les fronts.
Voir aussi
Liens internes
Liens externes
- (en) Symbol Report: SOX6
Références
- COHEN-BARAK, Orit et al. : Sox6 regulation of cardiac myocyte development, Oxford University Press, 2003 PMID 14530442
- CONNOR, Frances et al. : The Sry-related HMG box-containing gene Sox6 is expressed in the adult testis and developing nervous system of the mouse, Oxford University Press, 1995 PMID 7567444
- DENNY, Paul et al. : A conserved family of genes related to the testis determining gene, SRY, Oxford University Press, 1992 PMID 1614875
- DUMITRIU, Bogdan et al. : Sox6 cell-autonomously stimulates erythroid cell survival, proliferation, and terminal maturation and is thereby an important enhancer of defenitive erythropoiesis during mouse development, Blood, 2006 PMID 16627753
- HAGIWARA, Nobuko et al. : Sox6 is a candidate gene for p100H myopathy, heart block, and sudden neonatal death, PubMed Central, 2000 PMID 10760285
- SMITS, Patrick et al. : The Trascription Factor L-Sox5 and Sox6 Are Essential for Cartilage Formation, ScienceDirect, 2001 PMID 11702786
- SMITS, Patrick et al. : Sox5 and Sox6 are needed to develop and maintain source, columnar, and hypertrophic chondrocytes in the cartilage growth plate, JCB, 2004 PMID 14993235
v · m | |||||
|---|---|---|---|---|---|
| Général | |||||
| Structure | |||||
| Classification |
| ||||
| Dosage colorimétrique | |||||
| Méthodes d'investigation des interactions | |||||
 Portail de la biochimie
Portail de la biochimie  Portail de la biologie cellulaire et moléculaire
Portail de la biologie cellulaire et moléculaire
- ↑ a b et c GRCh38: Ensembl release 89: ENSG00000110693 - Ensembl, May 2017
- ↑ a b et c GRCm38: Ensembl release 89: ENSMUSG00000051910 - Ensembl, May 2017
- ↑ « Publications PubMed pour l'Homme », sur National Center for Biotechnology Information, U.S. National Library of Medicine
- ↑ « Publications PubMed pour la Souris », sur National Center for Biotechnology Information, U.S. National Library of Medicine
















