Chlorotoluène
Le chlorotoluène ou chlorométhylbenzène est un composé aromatique de formule C7H7Cl. Il est constitué d'un cycle benzénique substitué par un groupe méthyle et un atome de chlore. Comme tous les benzènes disubstitués, il existe sous la forme de trois isomères structuraux, les composés ortho, méta et para, selon la position relative des deux substituants sur le cycle.
Le chlorure de benzyle, parfois appelé α-chlorotoluène, est un isomère des chlorotoluènes où le chlore est substitué sur le groupe méthyle, mais il n'est pas considéré à proprement parler comme un chlorotoluène.
Propriétés
| Chlorotoluène | |||
| Nom | 2-Chlorotoluène | 3-Chlorotoluène | 4-Chlorotoluène |
| Autres noms | 1-Chloro-2-méthylbenzène o-chlorotoluène orthochlorotoluène | 1-Chloro-3-méthylbenzène m-chlorotoluène métachlorotoluène | 1-Chloro-4-méthylbenzène p-chlorotoluène parachlorotoluène |
| Représentation |  | 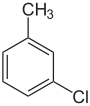 |  |
| Numéro CAS | 95-49-8 | 108-41-8 | 106-43-4 |
| 25168-05-2 (mélange d'isomères)[1] | |||
| ECHA | 100.002.205 | 100.003.255 | 100.003.089 |
| 100.042.438 (100.137.417) (mélange d'isomères) | |||
| PubChem | 6945 | 8489 | 7474 |
| Formule brute | C7H7Cl (C6H4ClCH3) | ||
| Masse molaire | 126,586 g mol−1 | ||
| État (CNTP) | liquide | ||
| Apparence | liquide incolore odeur aromatique[2] | liquide incolore odeur aromatique[3] | liquide incolore[4] |
| Point de fusion | −35 °C[2] | −48 °C[3] | 7,5 °C[4] |
| Point d'ébullition | 159 °C[2] | 162 °C[3] | 162 °C[4] |
| Masse volumique (20 °C) | 1,08 g·cm-3[2] | 1,08 g·cm-3[3] | 1,07 g·cm-3[4] |
| Pression de vapeur saturante | 3,82 hPa (20 °C)[2] | 3,8 hPa (20 °C)[3] | 3,6 hPa (20 °C)[4] |
| Point d'éclair (coupelle fermée) | 43 °C[2] | 48 °C[3] | 49 °C[4] |
| Point d'auto-inflammation | > 550 °C[2] | > 550 °C[3] | 570 °C[4] |
| Limites d'explosivité | 1,3 – 8,3 vol.% (68 – 435 g/m³)[2] | 1,3 – 8,3 vol.% (68 – 435 g/m³)[3] | 1,3 – 8,3 vol.% (68 – 435 g/m³)[4] |
| Solubilité (eau) | 0,05 g l−1 (20 °C)[2] | 0,106 g l−1 (25 °C)[3] | 0,11 g l−1 (25 °C)[4] |
| Coefficient de partage octanol/eau (LogP) | 3,42[2] | 3,28[3] | 3,33[4] |
| SGH |     [2] |    [3] |    [4] |
| Phrases H et P | H226, H332, H361d et H410 H226 : Liquide et vapeurs inflammables H332 : Nocif par inhalation H361d : Susceptible de nuire au fœtus. H410 : Très toxique pour les organismes aquatiques, entraîne des effets à long terme | H226, H332 et H411 H226 : Liquide et vapeurs inflammables H332 : Nocif par inhalation H411 : Toxique pour les organismes aquatiques, entraîne des effets à long terme | H226, H317, H332 et H411 H226 : Liquide et vapeurs inflammables H317 : Peut provoquer une allergie cutanée H332 : Nocif par inhalation H411 : Toxique pour les organismes aquatiques, entraîne des effets à long terme |
| P210, P273, P280, P310 et P304+P340 P210 : Tenir à l’écart de la chaleur/des étincelles/des flammes nues/des surfaces chaudes. — Ne pas fumer. P273 : Éviter le rejet dans l’environnement. P280 : Porter des gants de protection/des vêtements de protection/un équipement de protection des yeux/du visage. P310 : Appeler immédiatement un CENTRE ANTIPOISON ou un médecin. P304+P340 : En cas d'inhalation : transporter la victime à l’extérieur et la maintenir au repos dans une position où elle peut confortablement respirer. | P210, P273 et P304+P340+P312 P210 : Tenir à l’écart de la chaleur/des étincelles/des flammes nues/des surfaces chaudes. — Ne pas fumer. P273 : Éviter le rejet dans l’environnement. P304+P340+P312 : En cas d'inhalation : transporter la personne à l’extérieur et la maintenir dans une position où elle peut confortablement respirer. Appeler un CENTRE ANTIPOISON/un médecin en cas de malaise. | P273 et P280 P273 : Éviter le rejet dans l’environnement. P280 : Porter des gants de protection/des vêtements de protection/un équipement de protection des yeux/du visage. | |
Les chlorotoluènes se présentent sous la forme de liquide incolores, très peu solubles dans l'eau, ils peuvent cependant être dissous dans d'autres solvants organiques tels que le benzène, l'éthanol, l'éther, l'acétate d'éthyle ou le chloroforme. Les points de fusion des composés ortho et méta sont relativement proches, celui du composé para, qui a une symétrie bien plus grande, est en revanche bien plus élevé. Les points de vaporisation de trois isomères sont par contre eux tous très proches.
| Paramètres de l'Équation d'Antoine[5] log10(P) = A−(B/(T+C)) | ||||
| T (K) | A | B | C | |
| 2-Chlorotoluène | 278,4–432,5 | 4,48741 | 1768,105 | −38,389 |
| 3-Chlorotoluène | 277,9–435,5 | 4,48148 | 1807,576 | −32,105 |
| 4-Chlorotoluène | 278,7 K–435,5 | 4,47458 | 1795,293 | −34,380 |
Production
Les chlorotoluènes peuvent être préparés à partir des toluidines correspondantes via la réaction de Sandmeyer[6]. Un mélange de 2- et 4-chlorotoluènes est obtenu par chloration du toluène avec du chlore et du fer, formant du chlorure de fer(III) comme acide de Lewis.
Uses
Les chlorotoluènes sont utilisés comme solvants et comme produits intermédiaires dans la production de teintures, de produits phytosanitaires et de produits pharmaceutiques.
Les 2- et 4-chlorotoluene sont des précurseurs du chlorure de benzyle (ClC6H4CH2Cl), du benzaldéhyde (ClC6H4CHO) et du chlorure de benzoyle (ClC6H4C(O)Cl)[7].
Notes et références
- (de) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en allemand intitulé « Chlortoluole » (voir la liste des auteurs).
- ↑ Entrée « Chlorotoluene, mixed isomers » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 6 septembre 2020 (JavaScript nécessaire).
- ↑ a b c d e f g h i j k et l Entrée « 2-Chlorotoluene » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 6 septembre 2020 (JavaScript nécessaire).
- ↑ a b c d e f g h i j k et l Entrée « 3-Chlorotoluene » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 6 septembre 2020 (JavaScript nécessaire).
- ↑ a b c d e f g h i j k et l Entrée « 4-Chlorotoluene » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 6 septembre 2020 (JavaScript nécessaire).
- ↑ Stull, D.R.: Vapor Pressure of Pure Substances Organic Compounds, in: Ind. Eng. Chem. 39 (1947) 517–540, doi:10.1021/ie50448a022.
- ↑ (de) Organikum, Johann Ambrosius Barth, (ISBN 3-335-00343-8), p. 566
- ↑ Ullmann's Encyclopedia of Industrial Chemistry, Weinheim, Wiley-VCH, (DOI 10.1002/14356007.o06_o03), « Chlorinated Benzenes and Other Nucleus-Chlorinated Aromatic Hydrocarbons »
Voir aussi
- Chlorure de benzyle ou α-chlorotoluène
- Dichlorotoluène
- Trichlorotoluène
- Tétrachlorotoluène
- Pentachlorotoluène
| –F | –Cl | –Br | –I | |
|---|---|---|---|---|
| Benzène | Fluorobenzène | Chlorobenzène | Bromobenzène | Iodobenzène |
| Phénol (–OH) | Fluorophénol | Chlorophénol | Bromophénol | Iodophénol |
| Aniline (–NH2) | Fluoroaniline | Chloroaniline | Bromoaniline | Iodoaniline |
| Anisole (–OCH3) | Fluoroanisole | Chloroanisole | Bromoanisole | Iodoanisole |
| Toluène (–CH3) | Fluorotoluène | Chlorotoluène | Bromotoluène | Iodotoluène |
| Nitrobenzène (–NO2) | Fluoronitrobenzène | Chloronitrobenzène | Bromonitrobenzène | Iodonitrobenzène |
| Alcool benzylique (–CH2OH) | Alcool fluorobenzylique | Alcool chlorobenzylique | Alcool bromobenzylique | Alcool iodobenzylique |
| Benzaldéhyde (–CHO) | Fluorobenzaldéhyde | Chlorobenzaldéhyde | Bromobenzaldéhyde | Iodobenzaldéhyde |
| Acide benzoïque (–COOH) | Acide fluorobenzoïque | Acide chlorobenzoïque | Acide bromobenzoïque | Acide iodobenzoïque |
 Portail de la chimie
Portail de la chimie











